Genetika in diagnoza
SMA je dedna bolezen z dobro opredeljenim genetskim vzrokom.1-3
SMA je avtosomno recesivna genetska bolezen, pri kateri pride do delecije ali mutacije dveh SMN1 genov - po 1 od vsakega starša.4
Priporočljivo je presejalno testiranje prenašalcev5
Ker se SMA pojavlja v celotni populaciji, Ameriški kolegij za medicinsko genetiko in genomiko (ACMG) priporoča, da se presejalno testiranje ponudi vsem parom, ne glede na raso ali etnično pripadnost.
ACMG predlaga, da se presejalno testiranje izvede pred spočetjem ali zgodaj v nosečnosti, da se prenašalci genske mutacije lahko sprejmejo zavestno odločitev glede načrtovanja družine.
Molekularno genetsko testiranje je pomembno orodje za postavitev diagnoze spinalne mišične atrofije6, 7
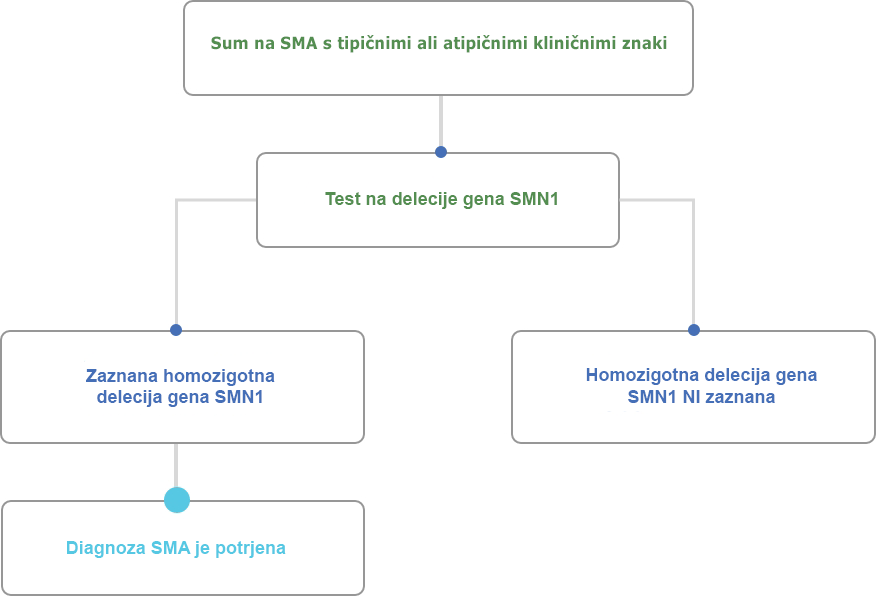
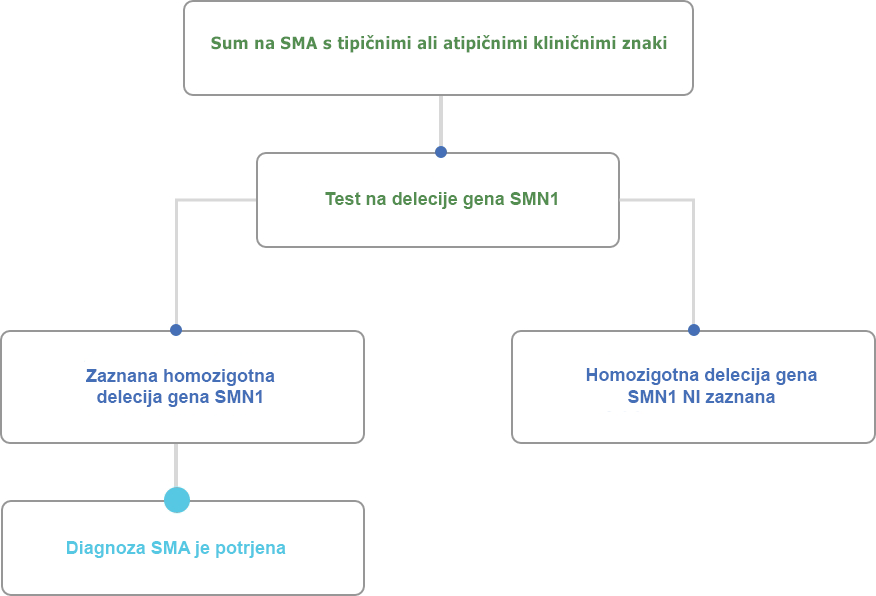
Povzeto po D`Amico et al.6
Test delecije gena SMN je priporočljiv kot prvi diagnostični postopek za bolnika, pri katerem obstaja sum na SMA.
Če se ugotovi, da ima bolnik eno kopijo gena SMN1 in je klinična prezentacija združljiva s SMA, lahko z nadaljnjim sekvencioniranjem preostalega gena SMN1 ugotovimo mutacije in potrdimo diagnozo SMA.7
Prikazane osebe so resnični bolniki. Bolniki in njihove družine so dali soglasje za uporabo njihovih zgodb. Fotografije so samo za ilustracijo.
SMA je rezultat homozigotnih delecij ali mutacij, ki vključujejo gen SMN v lokusu 5q13 kromosoma 5. Obstaja veliko redkih živčno-mišičnih bolezni (npr. Lambert-Eaton-ov miastenični sindrom, ki prizadene 0,05 - 0,08 / 100.000 ljudi na leto).8 Te bolezni lahko vključujejo mutacije različnih genov, ki niso povezani s 5q13.
Diferencialna diagnoza 5q spinalne mišične atrofije vključuje, ni pa omejena na:9
Bolezni hrbtenjače
- Neoplazme
- Ostale mielopatije
Miopatije
Prirojene miopatije:
- Prirojena miotonična distrofija
- Prirojene mišične distrofije
- Mišične distrofije
- Mitohondrijske miopatije
- Pompejeva bolezen
Ostale metabolne miopatije:
- Vnetne miopatije
- Kanalne miopatije
Nevropatije
- Prirojena hipomielinirajoča ali aksonska nevropatija
- Dedne motorične ali senzorične nevropatije
- Kronična vnetna demielinizirajoča polinevropatija
Bolezni živčno-mišičnih stikov
- Botulizem
- Prirojeni miastenični sindrom
- Lambert-Eatonov miastenični sindrom
- Avtoimunska miastenija gravis
Ostale bolezni motoričnega nevrona
- Spinalna mišična atrofija z dihalno stisko (SMARD)
- Juvenilna mišična atrofija distalne zgornje okončine (bolezen Hirayama)
- Fazio-Londejeva bolezen
- Brown-Vialetto-van Laere sindrom
- Juvenilna amiotrofična lateralna skleroza
- Ostale ne 5q SMA
Ostale bolezni
- Kromosomske nepravilnosti
- Prader-Willijev sindrom
- Abnormalnosti centralnega živčnega sistema
SMA je avtosomno recesivna genska bolezen3, 9
Spinalna mišična atrofija (SMA) je bolezen enega gena s spektrom različnih kliničnih prezentacij, ki se razlikuje glede na starost bolnika ob začetku bolezni in resnosti bolezni.7,17 Hipotonija ("floppy baby" sindrom) in / ali mišična šibkost in atrofija sta najpogostejša znaka ali simptoma bolezni pri otrocih.7,18
Gensko obolenje
Otrok podeduje dva izbrisana ali mutirana gena SMN1 -
po enega od vsakega starša4
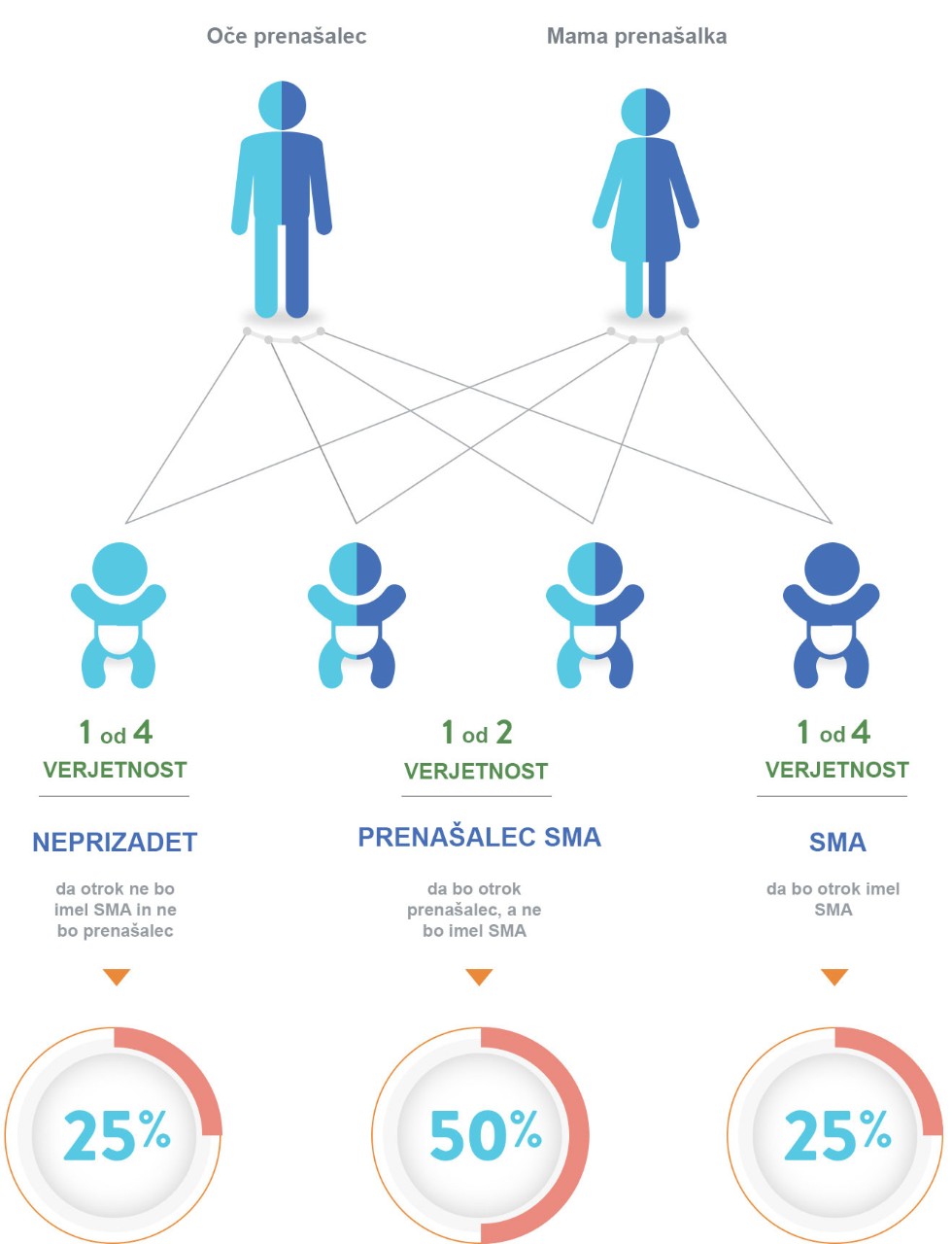
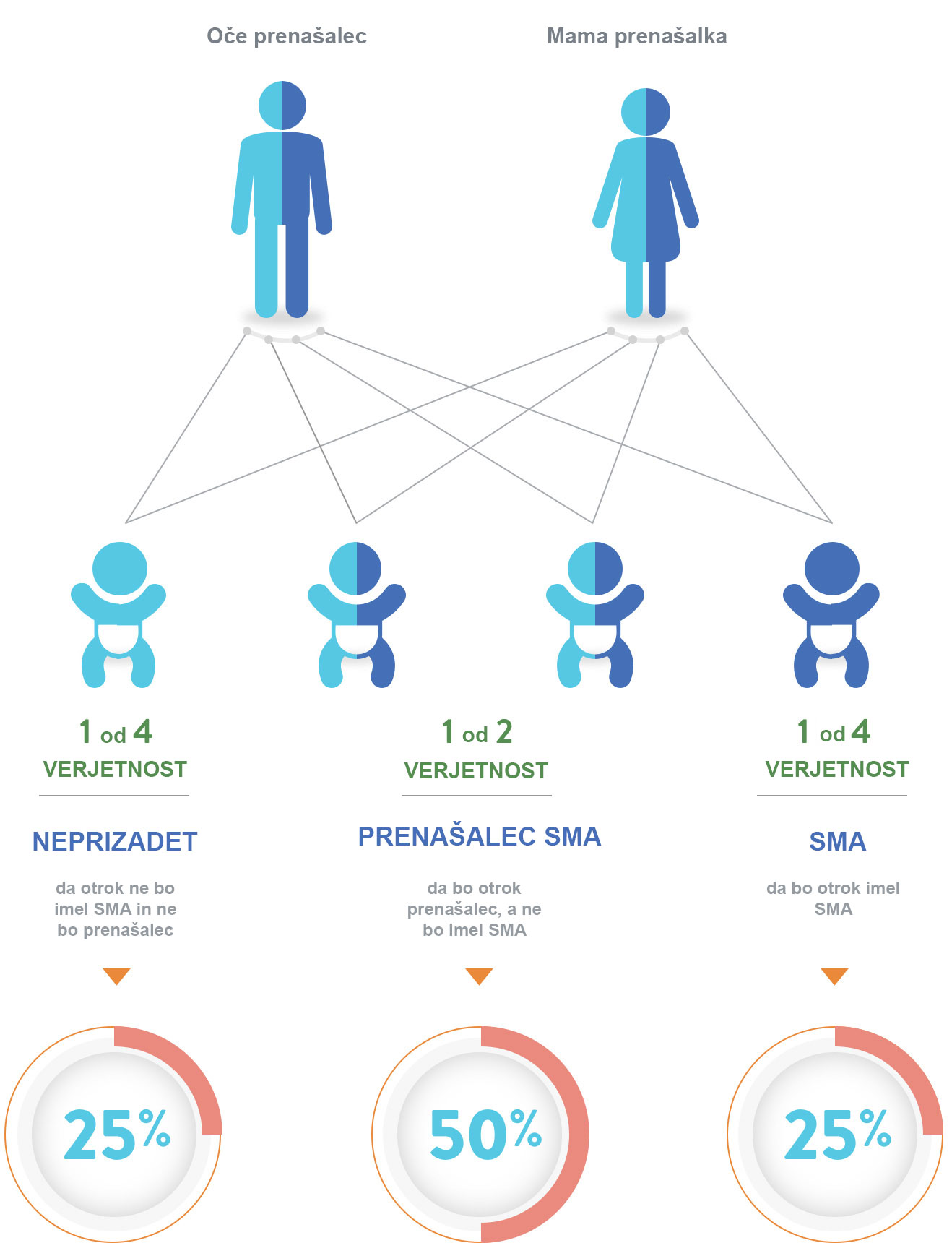
Pomen zgodnje postavitve diagnoze
Naravni potek SMA vključuje nepopravljivo izgubo motoričnih funkcij.8 Po sicer začetnem povečanju, začetek SMA označujeta vrh motoričnih sposobnosti in poznejši upad, pri čemer je napredovanje bolezni (in izguba motoričnih sposobnosti) najhitrejše v zgodnji fazi.19
Zgodnja postavitev diagnoze je lahko pomemben dejavnik pri zdravljenju SMA.20
![]() Vzorec izgube motoričnega nevrona, opažen pri SMA, kaže na to, da je treba zdravljenje pri infantilnem tipu SMA (tip 1) začeti čim prej, vključno že v pre-simptomatskim obdobju pred znatno izgubo motoričnih nevronov.20
Vzorec izgube motoričnega nevrona, opažen pri SMA, kaže na to, da je treba zdravljenje pri infantilnem tipu SMA (tip 1) začeti čim prej, vključno že v pre-simptomatskim obdobju pred znatno izgubo motoričnih nevronov.20
![]() Molekularno genetsko testiranje je pomembno orodje za postavitev diagnoze SMA.7, 21
Molekularno genetsko testiranje je pomembno orodje za postavitev diagnoze SMA.7, 21
Ocena oblike SMA
Za oceno naravnega poteka bolezni in odziva na zdravljenje je bilo razvitih več lestvic za oceno motoričnih funkcij.22-24


1. Lefebvre S, Bürglen L, Reboullet S, et al. Identification and characterization of a spinal muscular atrophy-determining gene. Cell 1995;80(1):155-165. | 2. Kolb SJ, Kissel JT. Spinal muscular atrophy. Arch Neurol 2011;68(8):979-984. | 3. Lunn MR, Wang CH. Spinal muscular atrophy. Lancet 2008;371(9630):2120-2133. | 4. National Organization for Rare Diseases. Spinal muscular atrophy. [online] 2012 [cited 2016 Apr 17]. Available from: URL: http://rarediseases.org/rarediseases/spinal-muscular-atrophy/. | 5. Prior TW; Professional Practice Guidelines Committee. Carrier screening for spinal muscular atrophy. Genet Med 2008;10(11):840-842. | 6. D’Amico A, Mercuri E, Tiziano FD, Bertini E. Spinal muscular atrophy. Orphanet J Rare Dis 2011;6:71. | 7. Mercuri E, et al. Diagnosis and management of spinal muscular atrophy: Part 1: Recommendations for diagnosis, rehabilitation, orthopaedic and nutritional care. Neuromuscl Disord 2018;28(2):103-115. | 8. Wirtz PW, Nijnuis MG, Sotodeh M, et al. The epidemiology of myasthenia gravis, Lambert–Eaton myasthenic syndrome and their associated tumours in the northern part of the province of South Holland. J Neurol. 2003;250(6):698–701. doi: 10.1007/ s00415-003-1063-7 | 9. Darras BT, Royden Jones H Jr, Ryan MM, De Vivo DC, eds. Neuromuscular Disorders of Infancy, Childhood, and Adolescence: A Clinician’s Approach. 2nd Ed. London, UK: Elsevier; 2015. | 16. Rothwell E, Anderson RA, Swoboda KJ, Stark L, Botkin JR. Public attitudes regarding a pilot study of newborn screening for spinal muscular atrophy. Am J Med Genet A 2013;161A(4):679-686. | 17. Prior TW, Russman BS. Spinal muscular atrophy. NCBI Bookshelf Web site. [online] 2019 Nov [Cited 2020 Oct 15]. Available from: URL: http://www.ncbi.nlm.nih.gov/books/NBK1352/?report=printable. | 18. MedlinePlus. Spinal muscular atrophy. [online] 2019 [cited 2021 Mar 1]. Available from: URL: https://medlineplus.gov/ency/article/000996.html. | 19. Swoboda KJ, et al. Perspectives on Clinical Trials in Spinal Muscular Atrophy. J Child Neurol. 2007;22:957-66. | 20. Finkel RS. Electrophysiological and motor function scale association in a pre-symptomatic infant with spinal muscular atrophy type I. Neuromuscul Disord 2013;23(2):112-115. | 21. D'Amico A, Mercuri E, Tiziano FD, Bertini E. Spinal muscular atrophy. Orphanet J Rare Dis. 2011;6:71. | 22. Glanzman AM, et al. The Children’s Hospital of Philadelphia Infant Test of Neuromuscular Disorders (CHOP INTEND): test development and reliability. Neuromuscul Disord 2010;20(3):155-161. | 23. Romeo DM, Ricci D, Brogna C, Mercuri E. Use of the Hammersmith Infant Neurological Examination in infants with cerebral palsy: a critical review of the literature. Dev Med Child Neurol 2016;58(3):240-245. | 24. Mercuri E, et al. Patterns of disease progression in type 2 and 3 SMA: implications for clinical trials. Neuromuscul Disord 2016;26(2):123-131. | 25. Spinal Muscular Atrophy Clinical Research Center. CHOP INTEND for SMA Type I score sheet. [online] 2013 Mar [cited 2016 Apr 26]. Available from: URL: http://columbiasma.org/docs/cme-2010/CHOP INTEND for SMA Type I - Manual of Procedures.pdf. | 26. The Pediatric Neuromuscular Clinical Research Network for SMA. Expanded Hammersmith Functional Motor Scale for SMA (HFMSE). [online] 2009 Mar [cited 2016 Apr 25]. Available from: URL: http://columbiasma.org/docs/HFMSE_2019_Manual.pdf.
Biogen-122894 I Junij 2022
